IA en el hospital:
Implementala para optimizar tiempos y aumentar la seguridad clínica.
IA EN CLINICA
Minutos que ayudan vs. alertas que sobran
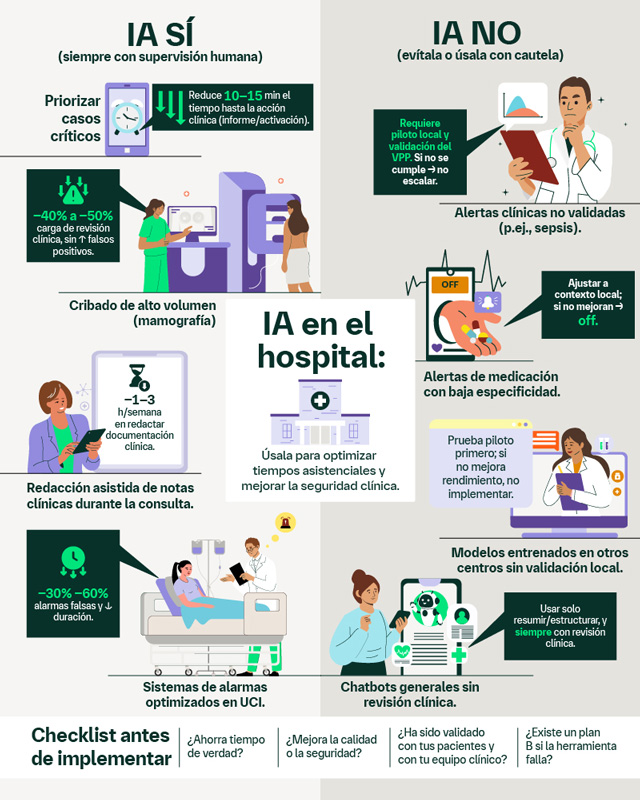
La inteligencia artificial ya forma parte de hospitales y consultas, pero no todas las aplicaciones aportan el mismo valor. En términos generales, funciona mejor cuando automatiza tareas repetitivas, prioriza casos críticos o estructura la información, y rinde peor cuando genera alertas imprecisas, no está validada localmente o se utiliza sin supervisión humana (especialmente en modelos generativos). Esta no es una promesa futurista: la IA ya está entrando en consultas, en servicios de radiología y en UCI, con resultados tangibles, aunque heterogéneos. Aporta más cuando acelera los cuellos de botella claros, por ejemplo, la priorización de estudios urgentes o la reducción de la carga documental, y se integra en equipos y circuitos clínicos bien definidos. Por el contrario, pierde utilidad cuando dispara demasiadas alertas de bajo valor, carece de validación en la población y flujo locales, o se emplea sin revisión humana explícita. La OMS ha establecido un marco de gobernanza para grandes modelos multimodales que subraya la validación, la transparencia y la supervisión humana antes de escalar su uso asistencial1.
El valor “aquí y ahora” se evidencia con claridad en la imagen médica. Los sistemas que detectan hallazgos críticos y reordenan la lista de trabajo permiten que los casos verdaderamente urgentes sean valorados antes; en ictus por oclusión de gran vaso, acortar los minutos puede traducirse en decisiones terapéuticas más rápidas y equipos mejor coordinados. La evidencia reciente en entornos reales respalda esa ganancia operativa cuando la priorización se integra con avisos al equipo y protocolos de activación2.
También hay avances consistentes en el cribado de alta carga, como la mamografía. El ensayo MASAI demostró que la lectura asistida por IA mantiene tasas de detección comparables a la doble lectura y, a la vez, reduce sustancialmente el volumen a revisar (≈ 44 % menos de carga)3. Este beneficio, menos trabajo repetitivo sin pérdida de calidad, es exactamente lo que buscan los programas poblacionales; además, estudios posteriores en programas reales indican que puede aumentar la detección sin penalizar los falsos positivos, siempre que la implementación sea cuidadosa.
En paralelo, las herramientas de “documentación ambiental” empiezan a aliviar un dolor crónico: el tiempo dedicado a los registros médicos electrónicos. Los scribes de IA escuchan (con consentimiento) la entrevista clínica y generan un borrador estructurado de la nota. En evaluaciones multicéntricas, se asocian con menos tiempo de tecleo y menor carga percibida por parte del profesional4. La promesa no es magia: es quitar la fricción administrativa para que la interacción clínico- paciente recupere tiempo y atención.
La detección precoz del deterioro intrahospitalario es otro ámbito en el que las señales son útiles cuando la IA no actúa sola, sino como parte de una intervención organizada (puntuación + circuito de respuesta). Un estudio de 2024 observó una disminución del riesgo de escaladas de cuidados tras implementar un modelo de deterioro habilitado por IA, lo que respalda la idea de que el impacto se observa cuando el algoritmo activa un proceso asistencial claro y medible2.
En UCI, la gestión “inteligente” de alarmas combina reglas clínicas y algoritmos para reducir las falsas alarmas y su duración. Esta mejora no solo combate la fatiga de las alarmas, un riesgo de seguridad bien documentado, sino que libera atención para lo verdaderamente relevante. Las revisiones recientes coinciden: la clave está en el ajuste fino a cada entorno, no en buscar un “algoritmo milagro”5.
¿Dónde conviene ir con más cautela? Un caso emblemático es la alerta de sepsis. Aunque muchos historiales médicos electrónicos incorporan avisos y el Epic Sepsis Model (ESM) se emplea en cientos de hospitales, este es un modelo propietario cuya información pública sobre su rendimiento es limitada. La validación externa independiente mostró un desempeño inferior al esperado y problemas de calibración, lo que recuerda que lo que funciona en un sitio no es transferible sin más a otro6. Ocurre algo similar con los sistemas de ayuda a la decisión farmacológica cuando las reglas son genéricas: si la mayoría de las alertas no son accionables, los profesionales las desactivan por hábito y la señal útil se diluye. Medir el valor predictivo positivo y la tasa de sobrelectura, ajustar los umbrales y contextualizar con datos clínicos suelen marcar la diferencia entre lo que ayuda y lo que puede introducir ruido.
Los grandes modelos de lenguaje merecen mención aparte. Aunque pueden resumir o estructurar información, su uso directo en decisiones clínicas, sin verificación humana, expone a sesgos y errores. La OMS pide una gobernanza específica: casos de uso acotados, trazabilidad de las salidas, controles de seguridad y, sobre todo, supervisión humana experta al final del proceso7.
Si tu hospital o servicio está valorando una herramienta, la pregunta no es “¿tiene IA?”, sino “¿resuelve nuestro cuello de botella de forma evidente y segura?”. Exigir datos locales de rendimiento y de impacto operativo (tiempos, carga, calidad), establecer umbrales de utilidad para las alertas, documentar el uso previsto y el plan de contingencia en caso de que la IA se abstenga o falle, y designar responsables clínicos que supervisen los resultados y los sesgos con el tiempo. La experiencia de los últimos años sugiere que la IA funciona cuando se comporta como una palanca de proceso y no como un oráculo: acelera lo urgente, ordena lo repetitivo y deja el juicio clínico exactamente dónde debe estar: en manos del profesional.
Lista de verificación antes de implementar

Validación en tu centro.
Comprueba que el sistema funciona con tu población, tus equipos (imagen, monitores, software) y tus circuitos clínicos. Realiza una prueba piloto breve con comparación antes/después y documenta los límites y posibles sesgos.

Beneficio operativo medible.
Define un objetivo concreto: por ejemplo, reducir los minutos de espera o de informe, disminuir el porcentaje de estudios por revisar o recortar el tiempo de registro. Si no hay una mejora clara o añades pasos, no escales su uso.

Seguridad y utilidad clínica.
Para sistemas con avisos, acuerda un umbral mínimo de utilidad (por ejemplo, valor predictivo positivo aceptable: proporción de alertas que realmente son correctas) y observa la tasa de desatención de las alertas (porcentaje que el clínico ignora o descarta). Establece seguimiento continuo y criterios de reversión si aumentan los falsos positivos o aparecen retrasos.

Gobernanza y responsabilidades.
Deja por escrito el uso previsto, cuándo el sistema debe abstenerse y el plan de contingencia (qué hacer si falla). Mantén la revisión humana obligatoria en tareas sensibles. Nombra a una persona responsable clínica y a otra de datos para revisar resultados y sesgos periódicamente.

Integración, privacidad y trazabilidad.
Integra la herramienta sin añadir clics innecesarios; registra la versión del modelo y las decisiones automatizadas. Aplica la minimización de datos, el consentimiento cuando proceda y la revalidación cada vez que se actualice el sistema.
Regla práctica: si no ahorra tiempo y no mejora la calidad o la seguridad, no justifica su implantación.
Infografía IA en la clínica
Referencias:
- https://www.who.int/news/item/18-01-2024-who-releases-ai-ethics-and-governance-guidance-for-large-multi-modal-models
- Gallo RJ, Shieh L, Smith M, et al. Effectiveness of an Artificial Intelligence–Enabled Intervention for Detecting Clinical Deterioration. JAMA Intern Med. 2024;184(5):557–562. doi:10.1001/jamainternmed.2024.0084v
- Artificial intelligence-supported screen reading versus standard double reading in the Mammography Screening with Artificial Intelligence trial (MASAI): a clinical safety analysis of a randomised, controlled, non-inferiority, single-blinded, screening accuracy study (2023). Lång, Kristina et al. The Lancet Oncology, Volume 24, Issue 8, 936 - 944
- Olson KD, Meeker D, Troup M, et al. Use of Ambient AI Scribes to Reduce Administrative Burden and Professional Burnout. JAMA Netw Open. 2025;8(10):e2534976. doi:10.1001/jamanetworkopen.2025.34976
- Mosch L, Sümer M, Flint AR, Feufel M, Balzer F, Mörike F, Poncette AS Alarm Management in Intensive Care: Qualitative Triangulation Study JMIR Hum Factors 2024;11:e55571. doi: 10.2196/55571
- Wong A, Otles E, Donnelly JP, et al. External Validation of a Widely Implemented Proprietary Sepsis Prediction Model in Hospitalized Patients. JAMA Intern Med. 2021;181(8):1065–1070. doi:10.1001/jamainternmed.2021.2626
- https://www.who.int/publications/i/item/9789240084759
DOC.7514.112025